实验介绍
高分子溶液与胶束的制备可从三个层次理解:微观上,是 F127 分子链段在不同溶剂环境中的构象转变;介观上,是分子间通过疏水作用力驱动的自组装过程,形成核-壳结构的纳米胶束;宏观上,则表现为原本不溶或难溶的药物在水中形成稳定的红色透明胶体溶液(表现出丁达尔效应)。
通过该方法,不仅显著提高了疏水药物的表观溶解度,同时利用 PEO 外壳实现对药物的空间屏蔽效应(“隐形”效应),从而赋予体系长循环特性,这是高分子纳米药物递送系统的重要优势。
嵌段共聚物自组装机理
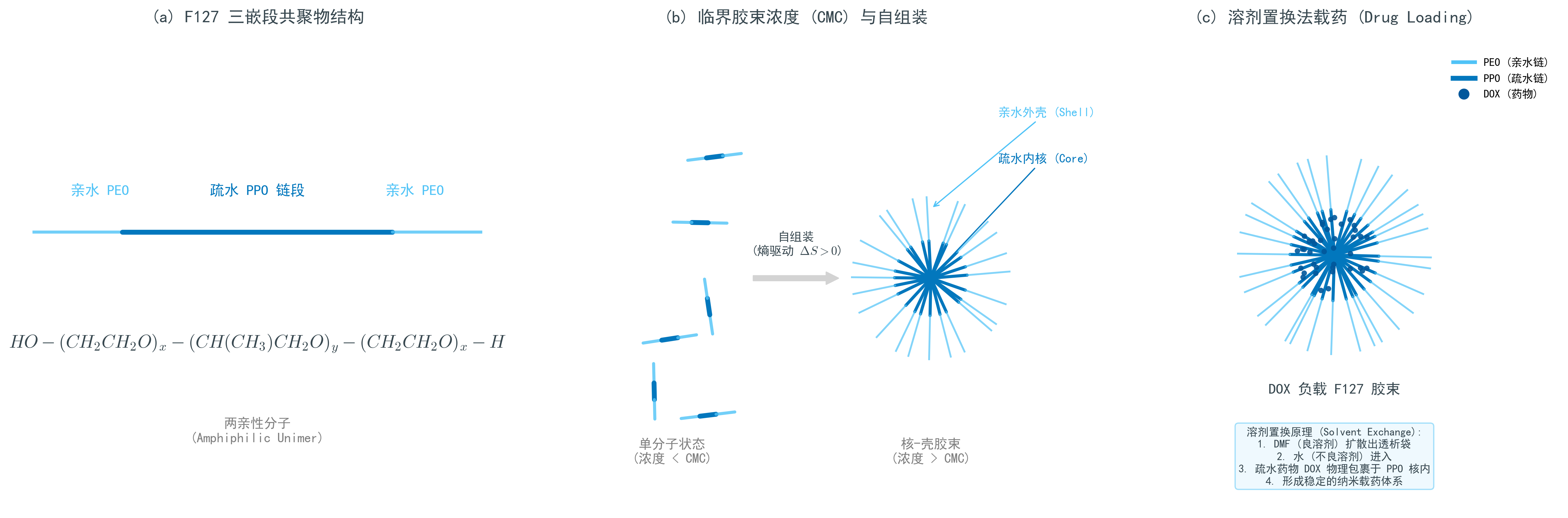
F127 胶束化与载药机理示意图
实验所用核心材料 F127 属于泊洛沙姆(Poloxamer)家族,为典型非离子型三嵌段共聚物,其结构为聚氧乙烯-聚氧丙烯-聚氧乙烯(PEO-PPO-PEO)。该结构由两端亲水的 PEO 链段与中间疏水的 PPO 链段构成,赋予分子两亲性。
PEO 链段富含醚键,可与水分子形成氢键,表现出良好的亲水性;PPO 链段由于含有侧基 $-CH_3$,极性较低且存在空间位阻,在水中表现出疏水性。F127 的结构通式为:
$$ \mathrm{HO-(CH_2-CH_2-O)_x-(CH(CH_3)-CH_2-O)_y-(CH_2-CH_2-O)_x-H} $$
其中,$x$ 和 $y$ 分别表示 PEO 与 PPO 的聚合度。其比例决定了材料的溶解性及相行为。
胶束形成是受热力学控制的自组装过程。当体系中聚合物浓度低于临界胶束浓度(CMC)时,分子以单链形式存在;当浓度超过 CMC 后,体系通过自组装形成胶束以降低自由能。
该过程满足:
$$ \Delta G = \Delta H - T \Delta S $$
胶束化主要由熵驱动:疏水链段暴露在水中时会诱导水分子形成有序结构,而当疏水链段聚集形成内核时,这些水分子被释放,使体系熵增加,从而满足:
$$ \Delta G < 0 $$
最终形成结构为:PPO 构成疏水内核,PEO 构成亲水外壳,依靠空间位阻稳定分散于水相中。
溶剂置换-透析法制备载药胶束
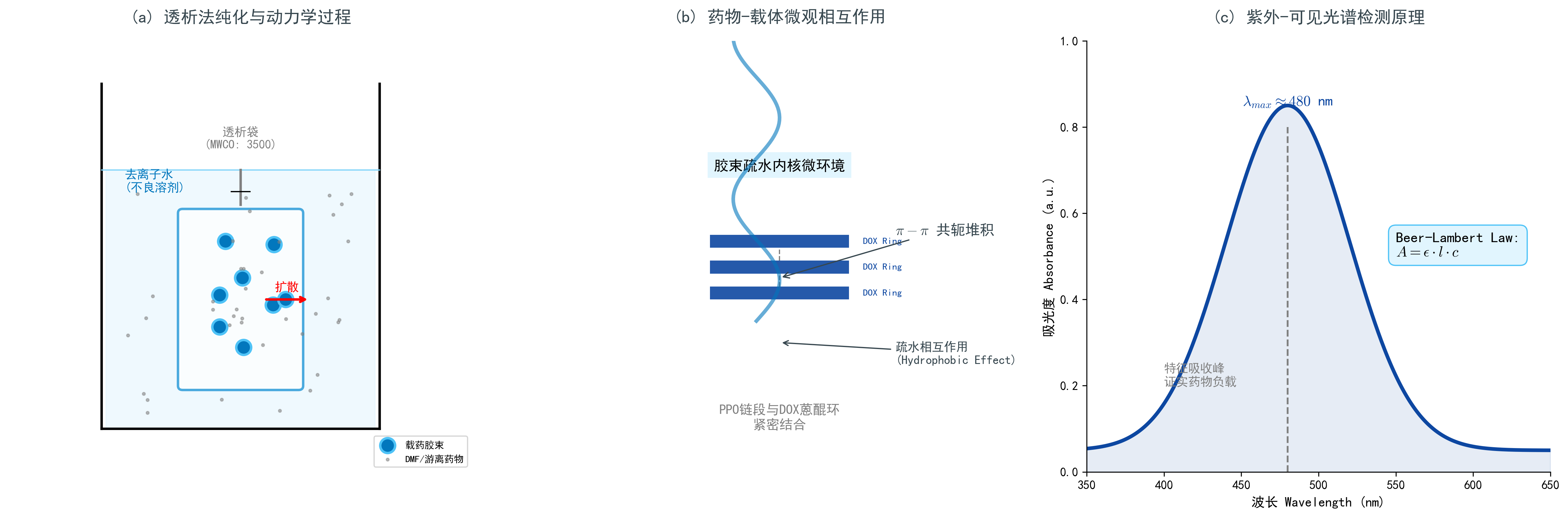
制备工艺与光谱学原理示意图
制备过程与动力学机制
实验采用溶剂置换法结合透析技术。首先将 F127 与阿霉素(DOX)溶解于 DMF 中,形成均一溶液。DMF 作为共溶剂,可同时溶解聚合物与疏水药物。
将该溶液缓慢滴加至去离子水中后,体系极性迅速提高。水为 PEO 的良溶剂,但对 PPO 与 DOX 为不良溶剂。随着 DMF 被稀释,PPO 链段发生塌缩并成核,同时 DOX 分子在“相似相溶”驱动下进入疏水微区。
随着结构稳定化,DOX 被包裹于 PPO 内核中,而 PEO 外壳维持其在水中的分散稳定性。
透析纯化过程
透析袋为半透膜,仅允许小分子(DMF、游离 DOX)通过,而截留胶束(粒径约 $10\sim100\ \mathrm{nm}$)。在浓度梯度驱动下:
- DMF 向外扩散
- 水向内渗透
- 游离 DOX 被去除
最终获得纯化的载药胶束体系。
药物包载与光谱检测原理
DOX 为蒽环类抗生素,分子包含疏水蒽醌环与亲水氨基糖结构。在胶束形成过程中,由于疏水作用及 $\pi-\pi$ 堆积作用,DOX 优先进入 PPO 内核或核-壳界面区域。
其检测基于比尔-朗伯定律:
$$ A = \log_{10}\left(\frac{I_0}{I}\right) = \epsilon \cdot l \cdot c $$
其中,$A$ 为吸光度,$\epsilon$ 为摩尔吸光系数,$l$ 为光程,$c$ 为浓度。
DOX 在约 $480\ \mathrm{nm}$ 处发生 $\pi \rightarrow \pi^\ast$ 跃迁,产生特征吸收峰。F127 在 $400\sim800\ \mathrm{nm}$ 区间无吸收,因此该波长可用于特异性检测药物包载情况。
实验指标分析
空白胶束表征
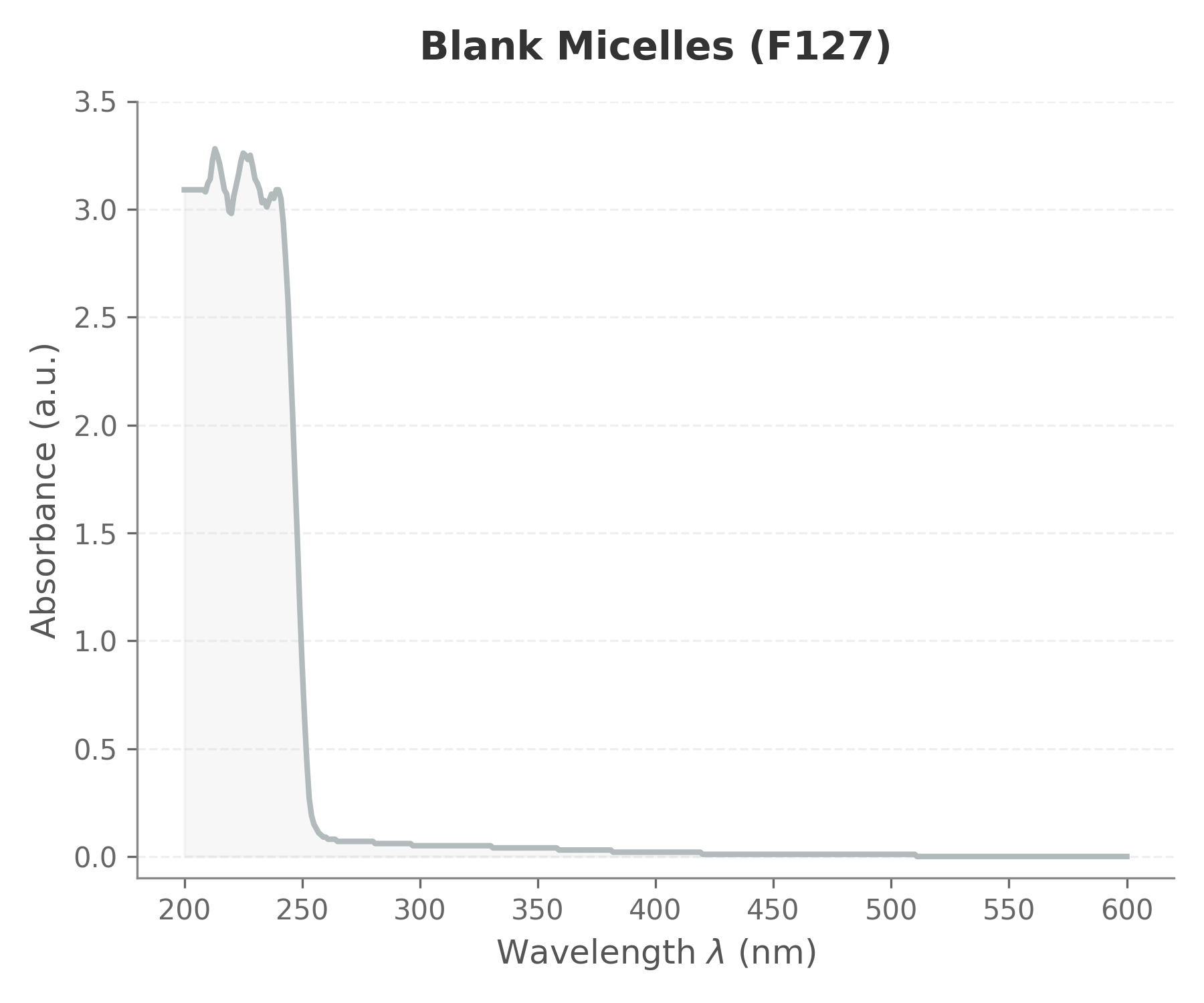
空白胶束的 Abs 谱图
空白胶束在 $200\sim220\ \mathrm{nm}$ 区域存在吸收峰,而在 $400\sim600\ \mathrm{nm}$ 区间吸光度接近于 0($A<0.05$)。说明:
- F127 在检测波段无干扰
- 胶束体系分散性良好
- 无明显大尺寸聚集体
载药胶束的光谱特性
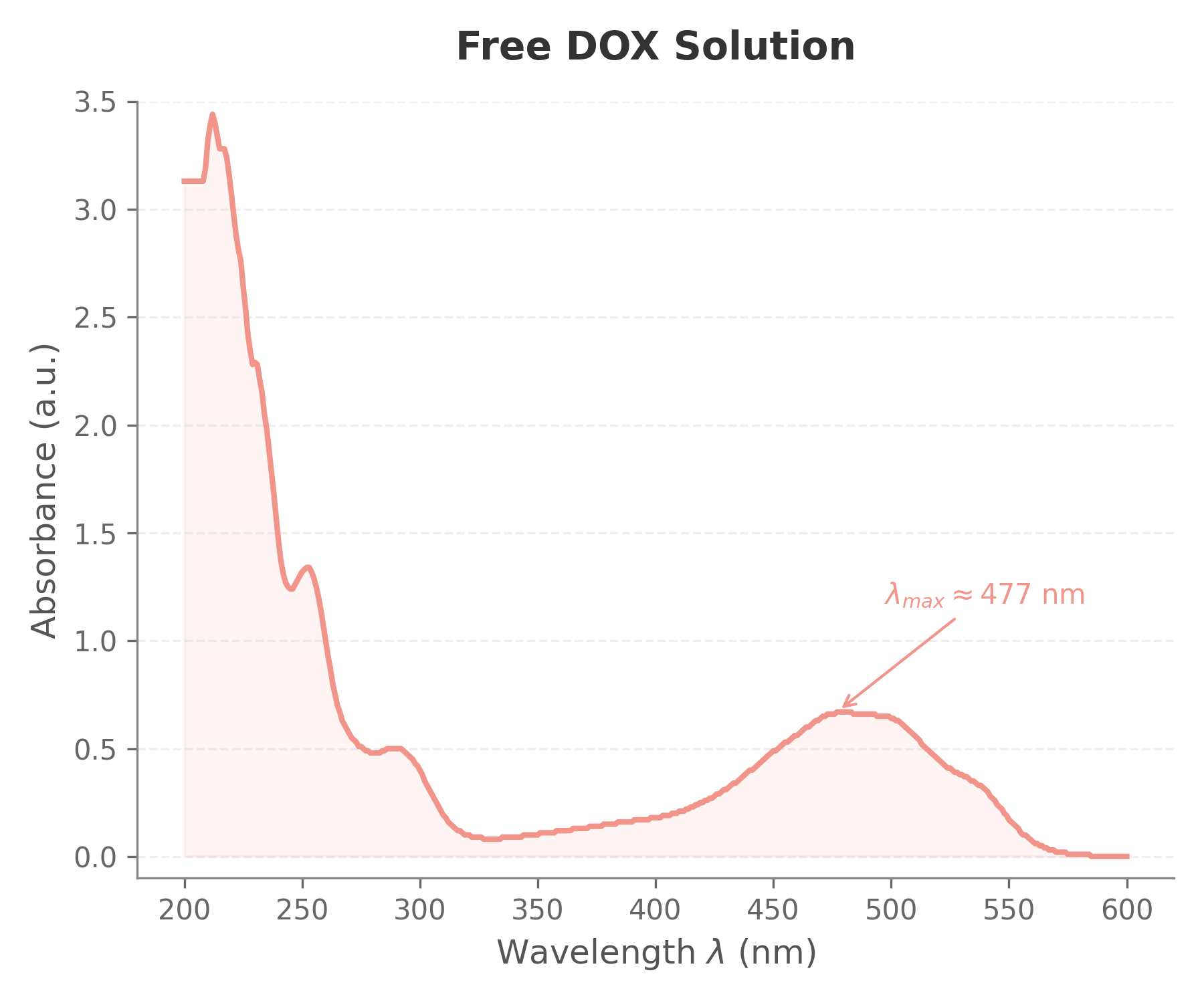
自由 DOX 的 Abs 谱图
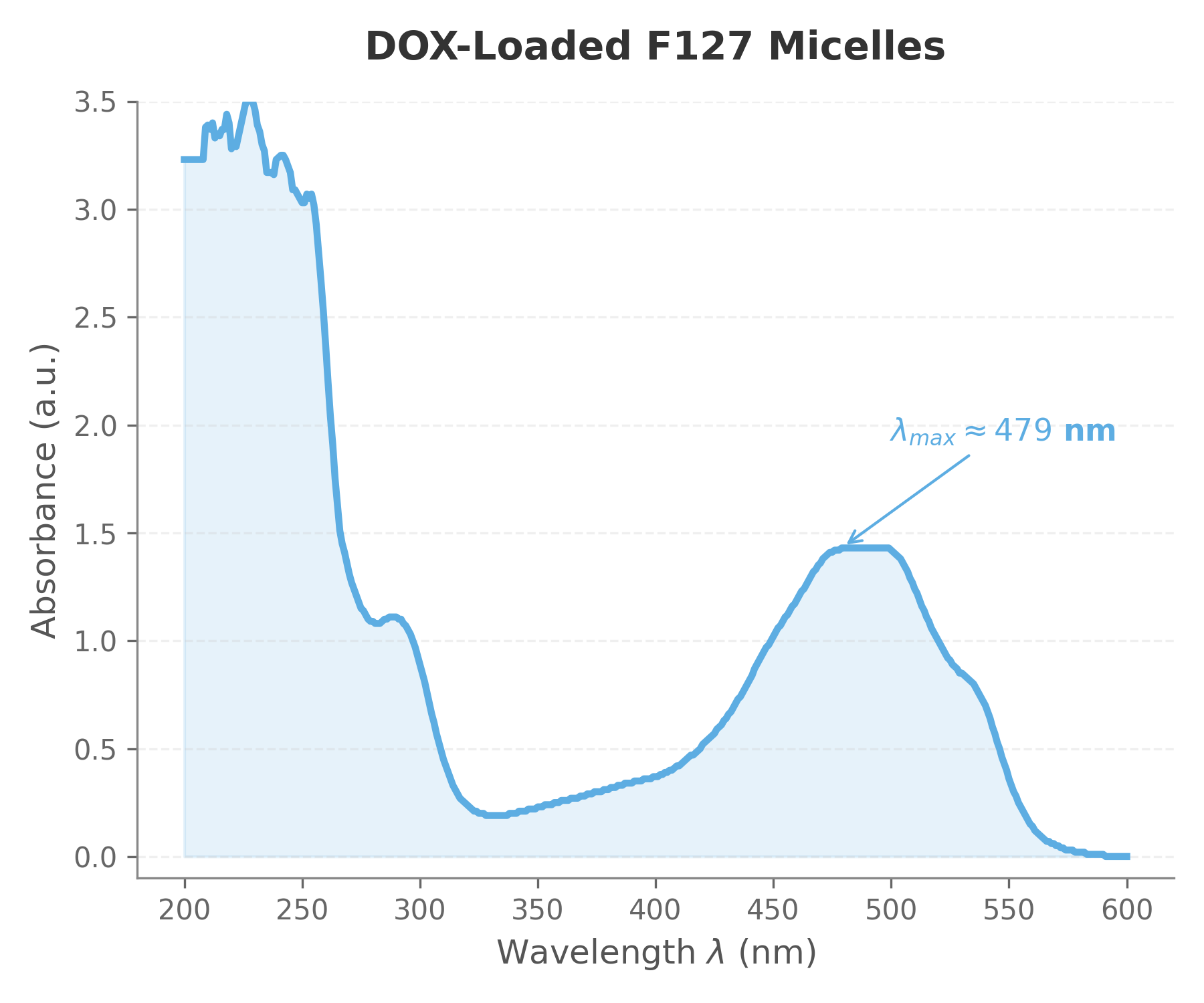
载药胶束的 Abs 谱图
游离 DOX 在 $480\sim500\ \mathrm{nm}$ 处具有特征吸收峰($\lambda_{\max} \approx 480\ \mathrm{nm}$)。载药胶束样品表现出相似峰位($\lambda_{\max} \approx 485\ \mathrm{nm}$),且吸光度增强(约 $1.43$ a.u.)。
由于透析已去除游离 DOX,因此该信号来源于被胶束包载的药物。
光谱对比与结构验证
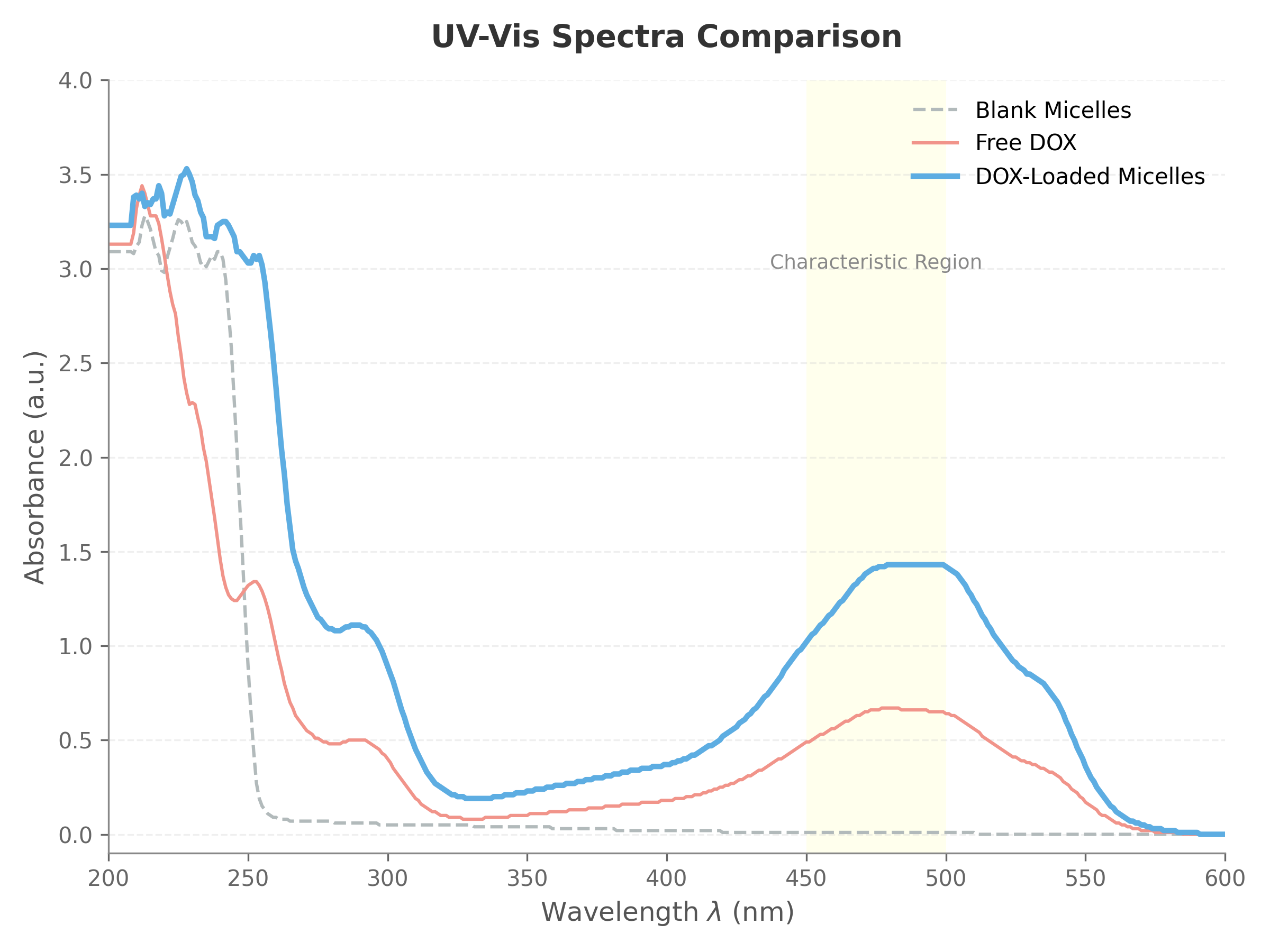
对比总谱图
载药体系相较游离 DOX 出现轻微红移($480 \rightarrow 485\ \mathrm{nm}$)。该现象表明 DOX 所处环境由极性水相转变为相对非极性的 PPO 内核环境,验证药物进入胶束内部。
实验结论
基于溶剂置换-透析法成功构建 F127-DOX 载药胶束体系。UV-Vis 光谱结果表明:
- 药物已成功包载于胶束内部
- 游离药物已有效去除
- 胶束体系具有良好的结构稳定性
该体系符合嵌段共聚物自组装载药的基本理论预期,可作为疏水药物递送的有效模型体系。
作者:GARFIELDTOM
邮箱:coolerxde@gt.ac.cn